一、目的:
二、适用范围:
本规程规定了培养基适用性检查方法和操作要求,适用于微生物实验室计数用培养基、控制菌检查用培养基的适用性检查。
三、内容:
1、简述
1.1 培养基适用性检查试验可用于确定实验室所使用培养基(包括购置的不同批号的成品培养基、不同批号的脱水培养基、按处方自行配制培养基所用不同批次的原材料等)、制备程序(包括水质控制、配制方法、灭菌程序等)、保存条件(温度、湿度、时间及盛装培养基的容器条件等)等是否满足微生物限度检查要求。
1.2 计数用培养基适用性检查包括需氧菌、霉菌及酵母菌总数计数。
1.3 控制菌检查用培养基适用性检查包括促生长能力、抑制能力及指示特性的检查。
2 计数用培养基适用性检查
微生物限度检查中计数用培养基有5种,胰酪大豆胨琼脂培养基、沙氏葡萄糖琼脂培养基、R2A琼脂培养基、平板计数培养基。
2.1 培养基及配制
2.1.1 培养基:胰酪大豆胨琼脂培养基、胰酪大豆胨琼脂对照培养基;沙氏葡萄糖琼脂培养基、沙氏葡萄糖琼脂对照培养基;R2A琼脂培养基、R2A琼脂对照培养基;平板计数培养基。
2.1.2 配制:照《培养基配制标准操作规程》配制。
2.2 试剂及稀释剂配制
2.2.1 试剂:pH7.0氯化钠-蛋白胨缓冲液、聚山梨酯80、氯化钠。
2.2.2 稀释剂配制
Ø pH7.0无菌氯化钠-蛋白胨缓冲液:称取pH7.0无菌氯化钠-蛋白胨缓冲液14.63g,加水1000mL溶解,分装,灭菌(121℃、15min)。
Ø 0.05%(mL/mL)聚山梨酯80的pH7.0无菌氯化钠-蛋白胨缓冲液:取已经灭菌好的聚山梨酯80(1mL),加入pH7.0无菌氯化钠-蛋白胨缓冲液,摇匀,即得。
Ø 0.9%无菌氯化钠溶液:称取氯化钠9.0g,加水溶解使成1000mL,分装,灭菌(121℃、15min)。
3 试剂及消毒液配制
3.1 试剂
新洁尔灭溶液、84消毒液、苯酚、75%医用消毒酒精。
3.2 消毒液配制
3.2.1 84消毒液:取84消毒液1ml,加水60ml(1:60),摇匀即得。
3.2.2 0.1%新洁尔灭溶液:取新洁尔灭溶液20.4ml,加水至1000ml,摇匀,即得。
3.2.3 5%的苯酚溶液:称取苯酚5g,加水至100ml,摇匀,即得。
3.2.4 75%酒精棉球:取灭菌脱脂棉撕成小块并揉捏成团,置于广口瓶内,加入75% 医用消毒酒精,充分浸润,即得。
4 试验用菌株及菌液制备
4.1 试验用菌株
金黄色葡萄球菌(Staphylococcus aureus)[CMCC(B)26003]
铜绿假单胞菌(Pseudomonas aeruginosa)[CMCC(B)10104]
枯草芽孢杆菌(Bacillus s aureus)[CMCC(B)63501]
白色念珠菌(Candida albicans)[CMCC(F)98001]
黑曲霉(Aspergillus niger)[CMCC(F)98003]
4.2 菌液制备
4.2.1 仪器与用具
Ø 仪器:生化培养箱(30~35℃)、霉菌培养箱(20~25℃)、恒温水浴锅。
Ø用具:酒精灯、打火机、吸耳球、试管架、大试管(20×200mm、15×200mm)、锥形瓶、硅胶塞、刻度吸管(1mL、2mL、5mL/10mL)、吸管桶、接种环、培养皿(90mm)、不锈钢培养皿桶、不锈钢吸管桶、玻璃专用笔。
5 菌液制备方法
5.1 金黄色葡萄球菌菌液制备方法
5.1.1 用无菌接种取金黄色葡萄球菌斜面中底部菌落一环,在装有pH7.0无菌氯化钠-蛋白胨缓冲液10mL的试管内壁上轻轻摩擦,使环上的菌苔全部洗于溶液中,振摇混匀。
5.1.2 用1ml无菌吸管吸取上述均匀菌液0.1mL加入装有9.9mL pH7.0无菌氯化钠-蛋白胨缓冲液的试管中,混匀,作为10-1级。
5.1.3 以此类推,10倍递增稀释至每1ml含菌数不大于100cfu的菌悬液,备用。
5.2 枯草芽孢杆菌菌液制备方法
照金黄色葡萄球菌菌液制备方法同法操作。
5.3铜绿假单胞菌菌液制备方法
照金黄色葡萄球菌菌液制备方法同法操作。
5.4 白色念珠菌菌液制备方法。
5.4.1 用无菌接种取白色念珠菌斜面中底部菌落一环,在装有pH7.0无菌氯化钠-蛋白胨缓冲液10ml的试管内壁上轻轻摩擦,使环上的菌苔全部洗于溶液中,振摇混匀。
5.4.2 用1ml无菌吸管吸取上述均匀菌液0.1ml加入装有9.9ml pH7.0无菌氯化钠-蛋白胨缓冲液的试管中,混匀,作为10-1级。
5.4.3 以此类推,10倍递增稀释至每1ml含菌数不大于100cfu的菌悬液,备用。
5.5 黑曲霉液制备方法
5.5.1 取黑曲霉的斜面一支,加入20ml含0.05%(ml/ml)聚山梨酯80的pH7.0无菌氯化钠-蛋白胨缓冲液于上述斜面培养物中,将孢子洗脱。
5.5.2 用管口带有薄的无菌棉花的无菌吸管吸出全部孢子悬液,装入另外一支无菌试管中,混匀,作为原液。
5.5.3 用1ml无菌吸管从试管中吸取0.1ml至另一支装有9.9mlpH7.0无菌氯化钠-蛋白胨缓冲液的试管中,混匀,作为10-1级。
5.5.4 以此类推,10倍递增稀释至每1ml含菌数不大于100cfu的孢子悬液,备用。
5.6 注意事项
5.6.1 每一稀释级,均需制备2个菌数计数平皿。(每一稀释级取2个无菌平皿,每皿接种1ml菌液,铜绿假单胞菌、金黄色葡萄球菌、枯草芽孢杆菌倾注胰酪大豆胨琼脂培养基,混匀,凝固后于30~35℃培养箱培养18~24h,计数;白色念珠菌、黑曲霉倾注沙氏葡萄糖琼脂培养基中,混匀,凝固后于20~25℃培养箱培养96h,计数。
5.6.2 每递增一稀释级,必须另换一支吸管。
5.6.3 稀释时,吸管插入上一级试管内不低于液面2.5cm,反复吸吹数次。
5.6.4 吸液时,应先吸至高于吸管刻度上部少许,然后提起吸管,贴于试管内壁调整液量至刻度,吸管移至下一稀释试管的内壁近液面处(切勿接触液面)缓慢地放出全部试液。
5.6.5 所用稀释菌液吸管均需放入装有5%苯酚溶液的消毒缸内,24小时后才能洗涤。
5.6.6 菌悬液制备后,若在室温下放置应在2h内使用,若在2~8℃冰箱保存的菌悬液可以在24h内使用。黑曲霉孢子悬液可在2~8℃冰箱保存,在验证过的贮存期内使用。
6 计数用培养基的适用性检查
6.1 实验操作
6.1.1 胰酪大豆胨琼脂培养基
Ø 接种方法
分别接种不大于100cfu的金黄色葡萄球菌、铜绿假单胞菌、枯草芽孢杆菌、白色念珠菌、黑曲霉的菌悬液于无菌平皿中,倾注约20ml胰酪大豆胨琼脂培养基,每株试验菌平行制备2个平板,轻轻摇匀。用相应的对照培养基替代被检培养基进行上述实验。
Ø 适用性检查
将接种金黄色葡萄球菌、铜绿假单胞菌、枯草芽孢杆菌的培养皿、对照培养皿于30~35℃培养不超过3天;将接种白色念珠菌、黑曲霉的培养皿、对照培养皿于20~25℃培养不超过5天。
6.1.2 沙氏葡萄糖琼脂培养基
Ø 接种方法
分别接种不大于100cfu的白色念珠菌、黑曲霉的菌悬液于无菌平皿中,倾注约20ml沙氏葡萄糖琼脂培养基,每株试验菌平行制备2个平板,轻轻摇匀。用相应的对照培养基替代被检培养基进行上述实验。
Ø 适用性检查
将接种白色念珠菌、黑曲霉培养皿、对照培养皿于20~25℃培养不大于5天。
6.1.3 R2A琼脂培养基
Ø 接种方法
分别接种不大于100cfu的铜绿假单胞菌、枯草芽孢杆菌的菌悬液于无菌平皿中,倾注约20mlR2A琼脂培养基,每株试验菌平行制备2个平板,轻轻摇匀。用相应的对照培养基替代被检培养基进行上述实验。
Ø 适用性检查
将接种铜绿假单胞菌、枯草芽孢杆菌的培养皿、对照培养皿于30~35℃培养不大于3天。
6.1.5 平板计数琼脂培养基
Ø 接种方法
分别接种不大于100cfu的金黄色葡萄球菌、铜绿假单胞菌、枯草芽孢杆菌、白色念珠菌、黑曲霉的菌悬液于无菌平皿中,倾注约15ml该培养基,每株试验菌平行制备2个平板,轻轻摇匀。用相应的对照培养基替代被检培养基进行上述实验。
Ø 适用性检查
将接种金黄色葡萄球菌、铜绿假单胞菌、枯草芽孢杆菌的培养皿、对照培养皿于30~35℃培养不超过3天;将接种白色念珠菌、黑曲霉的培养皿、对照培养皿于30~35℃培养不超过5天
6.2 观察与计算
Ø 观察被检培养基上铜绿假单胞菌、金黄色葡萄球菌、枯草芽孢杆菌、白色念珠菌、黑曲霉的菌落形态、大小与对照培养基上铜绿假单胞菌、金黄色葡萄球菌、枯草芽孢杆菌、白色念珠菌、黑曲霉的菌落形态、大小是否一致。
Ø 依次计算被检培养基上铜绿假单胞菌、金黄色葡萄球菌、枯草芽孢杆菌、白色念珠菌、黑曲霉的菌落平均数与对照培养基上铜绿假单胞菌、金黄色葡萄球菌、枯草芽孢杆、白色念珠菌、黑曲霉的菌落平均数的比值。
6.3 结果与判断
Ø 若被检固体上的菌落数平均数与对照培养基菌落数平均数的比值应在0.5~2范围内,且菌落形态大小应与对照培养基上的菌落一致,各菌适用性检查符合规定。
Ø 若被检固体上的菌落数平均数与对照培养基菌落数平均数的比值低于0.5~2范围,且菌落形态大小与对照培养基上的菌落不一致,则判断该培养基的适用性查不符合规定。
7 控制菌检查用培养基适用性检查
控制菌检查用培养基有液体培养基和固体培养基。
7.1 培养基及制备
Ø 培养基:脱水培养基、对照用培养基。
Ø 制备:照培养基配制规程新鲜配制。
7.2 试验用菌株及菌液制备
Ø 试验用菌株
大肠埃希菌(Escherichia coli)[CMCC(B)44102]
金黄色葡萄球菌(Staphylococcus aureus)[CMCC(B)26003]
枯草芽孢杆菌(Bacillus subtilis)[CMCCB(B)63501]
铜绿假单胞菌(Pseudomonas aeruginosa)[CMCC(B)10104]
沙门菌(Salmonella paratyphi B)[CMCC(B)50094]
白色念珠菌(Candida albicans)[CMCC(F)98001]
7.3 控制菌检查用培养基需要测试的能力及判断指标
7.3.1 液体培养基
Ø 促生长能力检查
取不大于100CFU的试验菌分别接种于被检培养基和对照培养基中,在相应控制菌检查规定的培养温度(30~35℃)或(42~44℃)及最短培养基时间下培养。与对照培养基比较,被检培养基中试验菌应生长良好,表现为液体培养基变浑浊。
Ø 指示特性检查
取不大于100CFU的试验菌分别接种于被检培养基和对照培养基中,在相应控制菌检查规定的培养温度(30~35℃)或(42~44℃)及最短培养基时间下培养。与对照培养基管比较,被检培养基中试验菌生长情况/指示剂反映情况应与对照培养基一致。
Ø 抑制能力检查
取不大于100CFU的试验菌分别接种于被检培养基和对照培养基中,在相应控制菌检查规定的培养温度(30~35℃)或(42~44℃)及最长培养基时间下培养,试验菌应不得生长。
7.3.2 固体培养基
Ø 促生长能力检查
取试验菌液(含菌数不大于100CFU)分别接种于被检培养基和对照培养基上,在相应控制菌检查规定的培养温度(30~35℃或(42~44℃))及最短培养基时间下培养。与对照培养基比较,被检培养基与对照培养基上生长的菌落大小、形态特征应一致。
Ø 指示特性检查
取试验菌液(含菌数不大于100CFU)分别接种于被检培养基和对照培养基上,在相应控制菌检查规定的培养温度(30~35℃)或(42~44℃)及最短培养基时间下培养。被检培养基上试验菌的菌落形态特征、菌落颜色及指示剂反应情况应与对照培养基一致。
Ø 抑制能力检查
取试验菌液(含菌数不少于100CFU)分别接种于被检培养基和对照培养基上,在相应控制菌检查规定的培养温度(30~35℃)或(42~44℃)及最长培养基时间下培养,试验菌应不得生长。
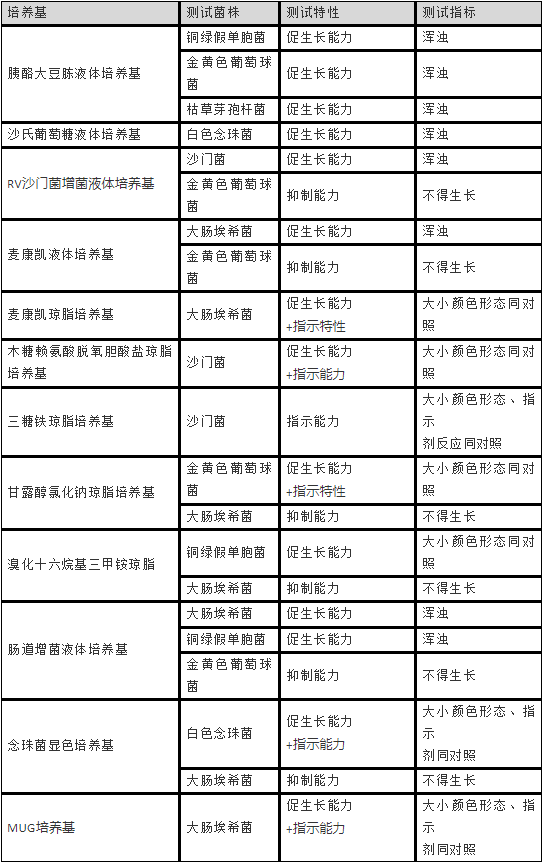
7.4 培养基能力测试列表
控制菌检查用培养基适用性检查项目、菌株及判断指标
7.5 实验操作
7.5.1 胰酪大豆胨液体培养基
Ø 促生长能力检查
接种方法:分别接种金黄色葡萄球菌、铜绿假单胞菌、枯草芽孢杆菌的菌悬液于该培养基中,接种量不大于100cfu,摇匀,培养。用相应的对照培养基替代被检培养基进行上述实验。
Ø 适用性检查:30~35℃培养不超过3天。
7.5.2 沙氏葡萄糖液体培养基
Ø 促生长能力检查
接种方法:接种白色念珠菌于该培养基中,接种量不大于100cfu,摇匀,培养。用相应的对照培养基替代被检培养基进行上述实验。
Ø 适用性检查:20~25℃培养不超过3天。
7.5.3 RV沙门菌增菌液体培养基
Ø 促生长能力检查
接种方法:分别接种不大于100cfu的沙门菌于被检培养基和对照培养基中。
适用性检查:在30~35℃条件下培养18~24h,与对照培养基管比较。
Ø 抑制能力检查
接种方法:分别接种不少于100cfu的金黄色葡萄球菌于被检培养基和对照培养基中。
Ø 适用性检查:在30~35℃条件下培养18~24h,并将被检培养基与对照培养基管
比较。
7.5.4 麦康凯液体培养基适用性检查
Ø 促生长能力检查
接种方法:分别接种不大于100cfu的大肠埃希菌于被检培养基和对照培养基中。
适用性检查:在42~44℃条件下培养18~24h,与对照培养基管比较。
Ø 抑制能力检查
接种方法:分别接种不少于100cfu的金黄色葡萄球菌于被检培养基和对照培养基
中。
Ø 适用性检查:在42~44℃条件下培养24h,并将被检培养基与对照培养基管比较。
7.5.5 麦康凯琼脂培养基适用性检查
Ø 促生长能力+指示特性的检查
接种方法:用涂布法分别接种不大于100cfu的大肠埃希菌于被检培养基和对照培养基平板上。
Ø 适用性检查:在30~35℃条件下培养18~24h。
7.5.6 木糖赖氨酸脱氧胆酸盐琼脂培养基
Ø 促生长能力+指示特性的检查
接种方法:用涂布法分别接种不大于100cfu的沙门菌于被检培养基和对照培养基平板上。
Ø 适用性检查:在30~35℃条件下培养18~24h。
7.5.7 三糖铁琼脂培养基、
Ø 指示能力
接种方法:用涂布法分别接种不大于100cfu的沙门菌于被检培养基和对照培养基高层斜面上,便进行穿刺。
Ø 适用性检查:在30~35℃条件下培养18~24h。
7.5.8 甘露醇氯化钠琼脂培养基
Ø 促生长能力+指示特性的检查
接种方法:用涂布法分别接种不大于100cfu的金黄色葡萄球菌于被检培养基和对照培养基平板上。
Ø 适用性检查:在30~35℃条件下培养18~24h。
Ø 抑制能力检查
接种方法:用涂布法分别接种不少于100cfu的大肠埃希菌于被检培养基和对照培养基平板上。
Ø 适用性检查:在30~35℃条件下培养18~24h,并将被检培养基与对照培养基比较。
7.5.9 溴化十六烷基三甲铵琼脂培养基
Ø 促生长能力检查
接种方法:用涂布法接种不大于100cfu的铜绿假单胞菌于被检培养基和对照培养
基平板上。
Ø 适用性检查:在30~35℃条件下培养18~24h,与对照培养基比较。
Ø 抑制能力检查
接种方法:用涂布法分别接种不少于100cfu的大肠埃希菌于被检培养基和对照培养基平板上。
Ø 适用性检查:在30~35℃条件下培养18~24h,并将被检培养基与对照培养基比较。
7.5.10 肠道菌增菌液体培养
Ø 促生长能力检查
接种方法:分别接种不大于100cfu的大肠埃希菌、铜绿假单胞菌于被检培养基和对照培养基中。
Ø 适用性检查:在30~35℃条件下培养18~24h,与对照培养基管比较。
Ø 抑制能力检查
接种方法:分别接种不少于100cfu的金黄色葡萄球菌于被检培养基和对照培养基中。
Ø 适用性检查:在30~35℃条件下培养18~24h,并将被检培养基与对照培养基管比较。
7.5.12 平板计数琼脂培养基
Ø 促生长能力检查
接种方法:用涂布法分别接种不大于100cfu的大肠埃希菌于被检培养基和对照培
养基平板上。
Ø 适用性检查:在30~35℃条件下培养18~24h,并将被检培养基与对照培养基比较。
Ø 抑制能力检查
接种方法:用涂布法分别接种不少于100cfu的金黄色葡萄球菌、枯草芽孢杆菌于被检培养基和对照培养基平板上。
Ø 适用性检查:在30~35℃条件下培养18~24h,并将被检培养基对照培养基比较。
7.5.13 念珠菌显色培养基
Ø 促生长能力检查
接种方法:用涂布法分别接种不大于100cfu的大肠埃希菌于被检培养基和对照培
养基平板上。
Ø 适用性检查:在30~35℃条件下培养18~24h,并将被检培养基与对照培养基比较。
Ø 抑制能力检查
接种方法:用涂布法分别接种不少于100cfu的金黄色葡萄球菌、枯草芽孢杆菌于被检培养基和对照培养基平板上。
Ø 适用性检查:在30~35℃条件下培养18~24h,并将被检培养基对照培养基比较。
7.5.14 MUG培养基
Ø 促生长能力+指示特性的检查
接种方法:分别接种不大于100cfu的大肠埃希菌于被检培养基和对照培养基平板中。
Ø 适用性检查:在30~35℃条件下培养18~24h。
8 注意事项
8.1 培养基的配制方法和灭菌程序发生变更时,应再次对培养基进行适用性检查。
8.2 培养基批号发生变更时,应再次对培养基进行适用性检查。
8.3 培养基供应商发生变更时,应再次对培养基进行适用性检查。
9 记录
每一次进行培养基的适用性检查后在《培养基适应性验证记录》上记录。








